Giải bài 1 trang 21 SGK Hóa 9
Bài 1: Có những oxit sau: SO2, CuO, Na2O, CO2. Hãy cho biết những oxit nào tác dụng được với:
a) Nước.
This post: Bài 5- Luyện tập- Tính chất hóa học của oxit và axit
b) Axit clohidric.
c) Natri hiđroxit?
Viết các phương trình hóa học.
Lời giải:
a) Những oxit tác dụng với nước: SO2, Na2O, CO2.
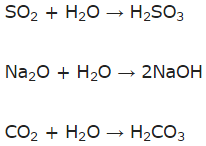
b) Những oxit tác dụng với dung dịch HCl: CuO, Na2O.
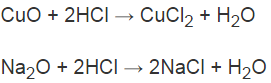
c) Những oxit tác dụng với dung dịch NaOH: CO2, SO2
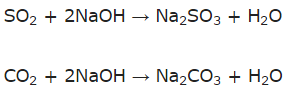
Giải bài 2 trang 21 SGK Hóa 9
Bài 2: Những oxit nào dưới đây có thể điều chế bằng:
a) Phản ứng hóa hợp? Viết phương trình hóa học.
b) Phản ứng hóa hợp và phản ứng phân hủy? Viết phương trình hóa học.
1) H2O.
2) CuO.
3) Na2O.
4) CO2.
5) P2O5.
c) Các oxit có thể điều chế bằng phản ứng hóa hợp và phản ứng phân hủy: CuO, CO2, Na2O, H2O
Lời giải:
a) Cả 5 oxit đã cho có thể điều chế bằng phản ứng hóa hợp. Viết các phương trình hóa học
2H2 + O2 −to→ 2H2O
2Cu + O2 −to→ 2CuO
4Na + O2 −to→ 2Na2O
4P + 5O2 −to→ 2P2O5
C + O2 −to→ CO2
b) Các oxit có thể điều chế bằng phản ứng hóa hợp và phản ứng phân hủy: CuO, CO2.
Cu(OH)2 −to→ CuO + H2O
2Cu + O2 −to→ 2CuO
CaCO3 −to→ CaO + CO2
2Ca + O2 −to→ 2CaO
c) Các oxit có thể điều chế bằng phản ứng hóa hợp và phản ứng phân hủy: CuO, CO2, Na2O, H2O
2NaNO2 −to→ Na2O + N2 + ½ O2
4Na + O2 −to→ 2Na2O
Ca(HCO3)2 −to→ CaCO3 + CO2 + H2O
2H2 + O2 −to→ 2H2O
Giải bài 3 trang 21 SGK Hóa 9
Bài 3: Khí CO được dùng làm chất đốt trong công nghiệp, có lẫn tạp chất là các khí CO2 và SO2. Làm thế nào có thể loại bỏ những tạp chất ra khỏi CO bằng hóa chất rẻ tiền nhất? Viết các phương trình hóa học xảy ra.
Lời giải:
Cho hỗn hợp khí CO, CO2, SO2 lội từ từ qua dung dịch Ca(OH)2. CO2 và SO2 tác dụng với dung dịch Ca(OH)2 (dư) tạo chất không tan CaCO3 và CaSO3 còn lại khí CO không tác dụng thoát ra.
CO2 + Ca(OH)2 → CaCO3 ↓ + H2O
SO2 + Ca(OH)2 → CaSO3 ↓ + H2O.
Giải bài 4 trang 21 SGK Hóa 9
Bài 4: Cần phải điều chế một lượng muối đồng sunfat. Phương pháp nào sau đây tiết kiệm được axit sunfuric:
a) Axit sunfuric tác dựng với đồng (II) oxit.
b) Axit sunfuric đặc tác dụng với kim loại đồng.
Giải thích cho câu trả lời.
Lời giải:
a) H2SO4 + CuO → CuSO4 + H2O (1)
b) Cu + 2H2SO4(đặc) → CuSO4 + SO2 ↑ + 2H2O (2)
Giả sử cần điều chế a mol CuSO4
Theo pt(1) nH2SO4 = nCuSO4 = a mol
Theo pt (2) nH2SO4 = 2.nCuSO4 = 2a mol
Do đó để tiết kiệm ta nên theo phản ứng (1) (phương pháp a) thì lượng axit H2SO4 sử dụng ít hơn ở phản ứng (2).
Giải bài 5 trang 21 SGK Hóa 9
Bài 5: Hãy thực hiện những chuyển đổi hóa học sau bằng cách viết những phương trình phản ứng hóa học (ghi điều kiện của phản ứng, nếu có).
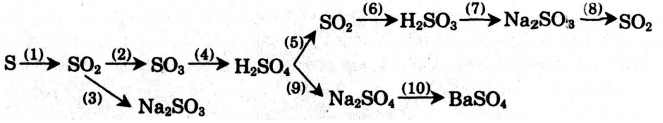
Lời giải:
Phương trình phản ứng:
1) S + O2 −to→ SO2
2) 2 SO2 + O2 −to,V2O5→ 2 SO3
3) SO2 + Na2 O → Na2SO3
4) SO3 + H2O → H2SO4
5) 2H2SO4 (đ) + Cu −to→ CuSO4 + SO2↑ + 2 H2O
6) SO2 + H2O → H2SO3
7) H2SO3 + 2 NaOH → Na2SO3 + 2H2O
8) Na2SO3 + 2HCl → 2 NaCl + SO2 ↑ + H2O
9) H2SO4 + 2 NaOH → Na2SO4 + 2H2O
10) Na2SO4 + BaCl2 → BaSO4 ↓ + 2 NaCl
Hóa học 9 Bài 5: Luyện tập: Tính chất hóa học của oxit và axit
I. Sơ đồ thể hiện tính chất chung của oxit
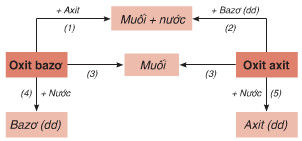
Bài tập Trắc nghiệm Hóa học 9 Bài 5 (có đáp án): Luyện tập: Tính chất hóa học của oxit và axit
Câu 1: Oxit axit là
A. Những oxit tác dụng với dung dịch axit tạo thành muối và nước.
B. Những oxit tác dụng với dung dịch bazơ tạo thành muối và nước.
C. Những oxit không tác dụng với dung dịch bazơ và dung dịch axit.
D. Những oxit chỉ tác dụng được với muối.
Hiển thị đáp án
Đáp án: B
Câu 2: Oxit trung tính là
A. Những oxit tác dụng với dung dịch axit tạo thành muối và nước.
B. Những oxit tác dụng với dung dịch bazơ tạo thành muối và nước.
C. Những oxit không tác dụng với axit, bazơ, nước.
D. Những oxit chỉ tác dụng được với muối.
Hiển thị đáp án
Đáp án: C
Câu 3: Chất tác dụng với nước tạo ra dung dịch axit là:
A. CaO
B. BaO
C. Na2O
D. SO3.
Hiển thị đáp án
Đáp án: D
Câu 4: Dãy oxit tác dụng với dung dịch axit clohiđric (HCl) là
A. CuO, Fe2O3, CO2, FeO.
B. Fe2O3, CuO, ZnO, Al2O3.
C. CaO, CO, N2O5, ZnO.
D. SO2, MgO, CO2, Ag2O.
Hiển thị đáp án
Đáp án: B
Câu 5: Hoà tan 23,5 g kali oxit vào nước được 0,5 lít dung dịch A. Nồng độ mol của dung dịch A là:
A. 0,25M.
B. 0,5M
C. 1M.
D. 2M.
Hiển thị đáp án
Đáp án: C
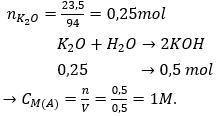
Câu 1: Oxit axit là
A. Những oxit tác dụng với dung dịch axit tạo thành muối và nước.
B. Những oxit tác dụng với dung dịch bazơ tạo thành muối và nước.
C. Những oxit không tác dụng với dung dịch bazơ và dung dịch axit.
D. Những oxit chỉ tác dụng được với muối.
Hiển thị đáp án
Đáp án: B
Câu 2: Oxit trung tính là
A. Những oxit tác dụng với dung dịch axit tạo thành muối và nước.
B. Những oxit tác dụng với dung dịch bazơ tạo thành muối và nước.
C. Những oxit không tác dụng với axit, bazơ, nước.
D. Những oxit chỉ tác dụng được với muối.
Hiển thị đáp án
Đáp án: C
Câu 3: Chất tác dụng với nước tạo ra dung dịch axit là:
A. CaO
B. BaO
C. Na2O
D. SO3.
Hiển thị đáp án
Đáp án: D
Câu 4: Dãy oxit tác dụng với dung dịch axit clohiđric (HCl) là
A. CuO, Fe2O3, CO2, FeO.
B. Fe2O3, CuO, ZnO, Al2O3.
C. CaO, CO, N2O5, ZnO.
D. SO2, MgO, CO2, Ag2O.
Hiển thị đáp án
Đáp án: B
Câu 5: Hoà tan 23,5 g kali oxit vào nước được 0,5 lít dung dịch A. Nồng độ mol của dung dịch A là:
A. 0,25M.
B. 0,5M
C. 1M.
D. 2M.
Hiển thị đáp án
Đáp án: C
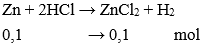
→ mmuối = 0,1. (65 + 71) = 13,6 gam.
Câu 10: Hòa tan hết hỗn hợp gồm CaO và CaCO3 cần vừa đủ 100 ml dung dịch HCl 3M. Khối lượng muối thu được là
A. 16,65 g
B. 15,56 g
C. 166,5 g
D. 155,6g
Hiển thị đáp án
Đáp án: A
Số mol HCl = 0,1.3 = 0,3 mol
Gọi số mol CaO là x mol; số mol CaCO3 là y mol
Ta có phương trình hóa học:
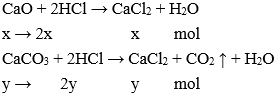
Theo PTHH có: nHCl = 2x + 2y = 0,3 mol → x + y = 0,15 mol
Muối thu được là CaCl2: (x + y) mol
→ mmuối = (x + y).(40 + 71) = 0,15.111=16,65 gam.
Bản quyền bài viết thuộc trường Mầm Non Ánh Dương. Mọi hành vi sao chép đều là gian lận.
Nguồn chia sẻ: Trường Mầm Non Ánh Dương (mamnonanhduongvt.edu.vn)
Source: Mamnonanhduongvt.edu.vn
Category: Giáo dục