Hợp chất hữu cơ là hợp chất của cacbon (trừ CO, CO2 muối cacbonat, xianua, cacbua,… không phải là hợp chất hữu cơ).
Vậy hợp chất hữu cơ là gì? phân loại hợp chất hữu cơ như thế nào? Đặc điểm chung của các hợp chất hữu cơ có gì khác với các hợp chất vô cơ? chúng ta cùng tìm hiểu qua bài viết dưới đây.
This post: Hợp chất hữu cơ là gì? Khái niệm, Phân loại và Đặc điểm chung của Hợp chất hữu cơ – Hóa 11 bài 20
I. Khái niệm về hợp chất hữu cơ và hóa học hữu cơ
– Hợp chất hữu cơ là hợp chất của cacbon (trừ CO, CO2, muối cacbonat, xianua, cacbua,…);
– Hóa học hữu cơ là ngành Hóa học nghiên cứu các hợp chất hữu cơ.
II. Phân loại hợp chất hữu cơ
• Có nhiề cách phân loại hợp chất hữu cơ, tuy nhiên, người ta hay dùng cách phân loại dựa theo thành phần các nguyên tố tạo nên hợp chất hữu cơ.
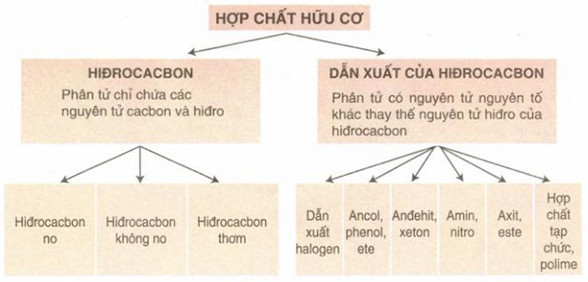
• Ngoài ra người ta còn phân loại hợp chất hữu cơ theo mạch cacbon:
– Hợp chất hữu cơ mạch vòng;
– Hợp chất hữu cơ mạch không vòng.
Trong mỗi loại lại được chia chi tiết hơn.
III. Đặc điểm chung của hợp chất hữu cơ
1. Đặc điểm cấu tạo
– Nguyên tố bắt buộc có trong hợp chất hữu cơ là cacbon
– Liên kết hóa học trong phân tử các hợp chất hữu cơ chủ yếu là liên kết cộng hoá trị.
2. Tính chất vật lí
– Các hợp chất hữu cơ thường có nhiệt độ nóng chảy, nhiệt độ sôi thấp (dễ bay hơi).
– Phần lớn các hợp chất hữu cơ không tan trong nước, nhưng tan nhiều trong các dung môi hữu cơ.
3. Tính chất hóa học
– Các hợp chất hữu cơ thường kém bền với nhiệt và dễ cháy.
– Phản ứng hóa học của các hợp chất hữu cơ thường xảy ra chậm và theo nhiều hướng khác nhau trong cùng một điều kiện, nên tạo ra hỗn hợp sản phẩm.
IV. Sơ lược về phân tích nguyên tố
– Để thiết lập công thức phân tử hợp chất hữu cơ, cần tiến hành phân tích định tính và định lượng các nguyên tố.
1. Phân tích định tính
a) Mục đích:
– Xác định nguyên tố nào có trong thành phần phân tử hợp chất hữu cơ.
b) Nguyên tắc:
– Chuyển các nguyên tố trong hợp chất hữu cơ thành các chất vô cơ đơn giản rồi nhận biết chúng bằng các phản ứng đặc trưng.
c) Phương pháp tiến hành:
– Trong phòng thí nghiệm, để xác định định tính cacbon và hiđro, người ta nung hợp chất hữu cơ với CuO để chuyển nguyên tố C thành CO2, nguyên tố H thành H2O.
– Phương pháp xác định nguyên tố N trong một số hợp chất đơn giản là chuyển nguyên tố N trong hợp chất hữu cơ thành NH3 rồi nhận biết bằng giấy quỳ tím ẩm.
2. Phân tích định lượng
a) Mục đích:
– Xác định thành phần phần trăm về khối lượng các nguyên tố trong phân tử hợp chất hữu cơ.
b) Nguyên tắc:
– Cân một khối lượng chính xác hợp chất hữu cơ, sau đó chuyển nguyên tố C thành CO2; nguyên tố H thành H2O; nguyên tố N thành N2,…
– Xác định chính xác khối lượng hoặc thể tích của các chất CO2, H2O, N2, … tạo thành, từ đó tính thành phần phần trăm khối lượng của các nguyên tố.
c) Phương pháp tiến hành:
– Để xác định thành phần phần trăm khối lượng các nguyên tố C, H, N, O trong chất hữu cơ, người ta tiến hành như sau:
– Nung một khối lượng chính xác (a gam) hợp chất hữu cơ chứa các nguyên tố H, O, N đã được trộn đều với bột CuO.
– Hấp thụ hơi H2O và khí CO2 lần lượt bằng H2SO4 đặc và KOH. Độ tăng khối lượng của mỗi bình chính là khối lượng H2O và CO2 tương ứng. Khí nitơ sinh ra được xác định chính xác thể tích và thường được quy về điều kiện tiêu chuẩn (đktc).
– Tính khối lượng H, C, N và phần trăm khối lượng của chúng trong hợp chất nghiên cứu. Từ đó tính được phần trăm khối lượng oxi.
d) Biểu thức tính:
 ;
; 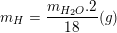 ;
; 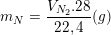
– Từ đó, ta tính được:
%C = 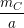 .100%; %H =
.100%; %H =  .100%; %N =
.100%; %N = 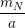 .100%;
.100%;
%O = 100% – %C – %H – %N.
– Hiện nay có các thiết bị hiện đại tự động phân tích phần trăm khối lượng của hầu hết các nguyên tố.
V. Bài tập về Hợp chất hữu cơ
* Bài 1 trang 91 SGK Hóa 11: So sánh hợp chất vô cơ và hợp chất hữu cơ về: thành phần nguyên tố, đặc điểm liên kết hoá học trong phân tử.
° Lời giải bài 1 trang 91 SGK Hóa 11:
• Về thành phần nguyên tố:
– Hợp chất hữu cơ là những hợp chất có chứa nguyên tố cacbon (trừ CO, CO2, muối cacbonat, xianiua, cacbua,…);
– Hợp chất vô cơ là những chất có thể có cacbon, có thể không. Hợp chất vô cơ chứa cacbon như CO, CO2, muối cacbonat, xianiua, cacbua,…
• Về đặc điểm liên kết hoá học trong phân tử:
– Hợp chất hữu cơ được cấu tạo chủ yếu từ các nguyên tố phi kim có độ âm điện khác nhau không nhiều.
– Liên kết trong hợp chất hữu cơ chủ yếu là liên kết cộng hoá trị.
– Hợp chất vô cơ được cấu tạo chủ yếu từ các nguyên tố kim loại với phi kim.
– Liên kết trong hợp chất vô cơ chủ yếu là liên kết ion.
* Bài 2 trang 91 SGK Hóa 11: Nêu mục đích và phương pháp tiến hành phân tích định tính và định lượng nguyên tố.
° Lời giải bài 2 trang 91 SGK Hóa 11:
• Phân tích định tính:
+ Mục đích:
– Xác định nguyên tố nào có trong thành phần phân tử hợp chất hữu cơ.
+ Phương pháp tiến hành:
– Trong phòng thí nghiệm, để xác định định tính cacbon và hiđro, người ta nung hợp chất hữu cơ với CuO để chuyển nguyên tố C thành CO2, nguyên tố H thành H2O.
– Phương pháp xác định nguyên tố N trong một số hợp chất đơn giản là chuyển nguyên tố N trong hợp chất hữu cơ thành NH3 rồi nhận biết bằng giấy quỳ tím ẩm.
• Phân tích định lượng:
+ Mục đích: Xác định thành phần phần trăm về khối lượng các nguyên tố trong phân tử hợp chất hữu cơ.
+ Phương pháp tiến hành:
– Nung một khối lượng chính xác (a gam) hợp chất hữu cơ chứa các nguyên tố H, O, N đã được trộn đều với bột CuO.
– Hấp thụ hơi H2O và khí CO2 lần lượt bằng H2SO4 đặc và KOH. Độ tăng khối lượng của mỗi bình chính là khối lượng H2O và CO2 tương ứng. Khí nitơ sinh ra được xác định chính xác thể tích và thường được quy về điều kiện tiêu chuẩn (đktc).
– Tính khối lượng H, C, N và phần trăm khối lượng của chúng trong hợp chất nghiên cứu. Từ đó tính được phần trăm khối lượng oxi.
* Bài 3 trang 91 SGK Hóa 11: Oxi hoá hoàn toàn 0,6 gam hợp chất hữu cơ A thu được 0,672 lít CO2 (đktc) và 0,72 gam H2O. Tính thành phần phần trăm khối lượng của các nguyên tố trong phân tử chất A.
° Lời giải bài 3 trang 91 SGK Hóa 11:
– Gọi Công thức phân tử của hợp chất hữu cơ là CxHyOz (x, y, z nguyên dương)
– Theo bài ra, ta có:
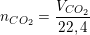
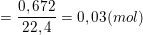
⇒ nC = nCO2 = 0,03(mol) ⇒ mC = 0,03.12 = 0,36(g).
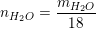
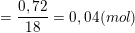
⇒ nH = 2.nH2O = 2.0,04 = 0,08(mol) ⇒ mH = 0,08.1 = 0,08(g).
– Suy ra số gam oxi có trong hỗn hợp:
mO = mhh – mC – mH = 0,6 – 0,36 – 0,08 = 0,16(g).
⇒ Hợp chất A có chứa C, H, O
– Phần trăm khối lượng các nguyên tố trong phân tử A là:
%C = 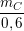 .100% =
.100% = 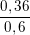 .100% = 60%
.100% = 60%
%H =  .100% =
.100% = 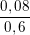 .100% = 13,33%
.100% = 13,33%
%O = 100% – 60% – 13,33% = 26,67%.
* Bài 4 trang 91 SGK Hóa 11: β-Caroten (chất hữu cơ có trong củ cà rốt) có màu da cam. Nhờ tác dụng của enzim ruột non, β-Croten chuyển thành vitamin A nên nó còn được gọi là tiền vitamin A. Oxi hoá hoàn toàn 0,67 gam β-Caroten rồi dẫn sản phẩm oxi hoá qua bình (1) đựng dung dịch H2SO4 đặc, sau đó qua bình (2) đựng dung dịch Ca(OH)2 dư. Kết quả cho thấy khối lượng bình (1) tăng 0,63 gam; bình (2) có 5 gam kết tủa. Tính phần trăm khối lượng của các nguyên tố trong phân tử β-Caroten
° Lời giải bài 4 trang 91 SGK Hóa 11:
– Ta có phương trình phản ứng hóa học:
Ca(OH)2 + CO2 → CaCO3↓ + H2O
– Khối lượng bình (1) tăng là khối lượng của H2O = 0,63(g) nên ta có:
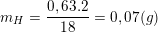
– Theo bài ra, khối lượng canxi cacbonat kết tủa là 5 (g) tức mCaCO3 = 5g
nên theo PTPƯ tac có: nCO2 = nCaCO3 = 5/100 = 0,05(mol).
⇒ nC = nCO2 = 0,05 (mol) ⇒ mC = 12. 0,05 = 0,6 (g).
⇒ mO = mhh – mC – mH = 0,67 – 0,6 – 0,07 = 0
⇒ %mC = (0,6/0,67).100% = 89,55%
%mH = (0,07/0,67).100% = 10,45%
Hy vọng với bài viết về Hợp chất hữu cơ: Khái niệm, Phân loại và Đặc điểm chung của Hợp chất hữu cơ ở trên hữu ích cho các em. Mọi thắc mắc và góp ý các em hãy để lại bình luận dưới bài viết để Mầm Non Ánh Dươngghi nhận và hỗ trợ, chúc các em học tốt!
Bản quyền bài viết thuộc trường Mầm Non Ánh Dương. Mọi hành vi sao chép đều là gian lận.
Nguồn chia sẻ: Trường Mầm Non Ánh Dương (mamnonanhduongvt.edu.vn)
Source: Mamnonanhduongvt.edu.vn
Category: Giáo dục





