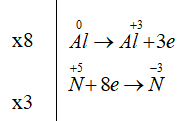Tính chất vật lý, tính chất hóa học của oxi và bài tập vận dụng
Nguyên tố oxi hay còn gọi là đơn chất phi kim oxi là một trong những vấn đề mà chúng ta đã tìm hiểu ở các lớp dưới cũng như trong đời sống hằng ngày. Tuy nhiên, dưới góc độ hóa học thì những kiến thức đó là chưa đủ. Chuyên mục Hóa Học sẽ giúp các em giải đáp về màu sắc, mùi, tính tan trong nước cũng như các tính chất vật lý và tính chất hóa học khác của oxi. Các em hãy cùng theo dõi nhé!
Nội dung chính
This post: Tính chất vật lý, tính chất hóa học của oxi và bài tập vận dụng
Tính chất vật lý của oxi
Theo một số thí nghiệm từ thực nghiệm về sự hòa tan oxi trong nước, chẳng hạn: 10 lít nước ở điều kiện 20 độ C thì chỉ hòa tan được 310ml khí Oxi. Hoặc thí nghiệm về độ nặng của khí oxi so với không khí bằng cách bơm vào bong bóng từ đó ta rút ra một số nhận xét về tính chất vật lý như sau:
Khí oxi (O2) là một chất khí không có màu sắc, không mùi vị, oxi ít tan trong nước và nặng hơn không khí. Nhiệt độ để oxi hóa lỏng là -183 độ và có màu xanh nhạt khi hóa lỏng.
Theo một số nghiên cứu thì khí oxi có tỉ khối so với không khí là: 32:29
Tính chất hóa học của oxi
Khi tìm hiểu bất kì một nguyên tốt hóa học nào, để hiểu hơn về cách ứng dụng vào lý thuyết cũng như các bài tập thì việc nắm vững tính chất hóa học là thật sự cần thiết. Dưới đây là 3 tính chất hóa học quan trọng nhất của oxi mà chúng ta cần nắm vững:
Oxi tác dụng với phi kim
Oxi tác dụng với khá nhiều phi kim trong tự nhiên và với những điều kiện khác nhau. Tuy nhiên trong chương trình hóa học 8 thì hai nguyên tố chúng ta cần nắm vững đó là: Ni-tơ (N) và Phốt-pho(P)
Tác dụng với lưu huỳnh (S)
Thực hiện thí nghiệm đốt cháy lưu huỳnh trong không khí ta rút ra một số kết luận sau:
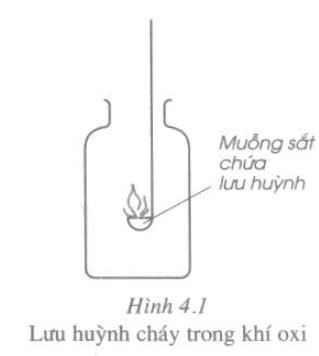
- Lưu huỳnh cháy trong Oxi mãnh liệt, ngọn lửa nhỏ màu xanh nhạt tạo thành khí lưu huỳnh đi-o-xít (SO2) và rất ít lưu huỳnh tri-o-xít (SO3)
- Phương trình hóa học:
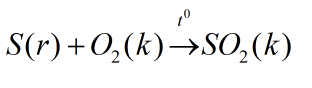
Tác dụng với Phốt – pho (P)
Thực hiện thí nghiệm sau ta rút ra một số kết luận sau:
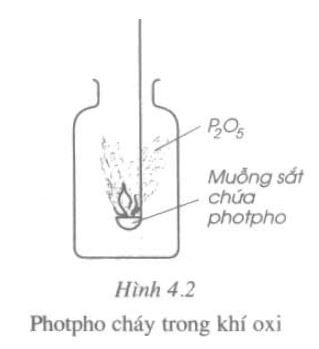
- Photpho cháy mạnh trong khí oxi với ngọn lửa sáng chói, tạo ra một lượng lớn khói trắng bám vào thành lọ. Bột trắng tan được trong nước và kí hiệu là P2O5 ( điphotpho pentaoxit)
- Phương trình hóa học:
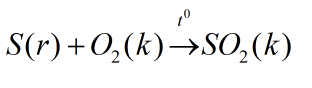
Oxi tác dụng với kim loại
Khác với phi kim, oxi khá kén chọn và khó xảy ra hơn. Tuy nhiên khi phản ứng với kim loại, Oxi phản ứng hầu hết và xảy ra kể cả trong điều kiện phức tạp cũng như điều kiện bình thường. Đương nhiên điều kiện bình thường phản ứng sẽ xảy ra lâu hơn – gỉ sắt là một minh chứng cho ví dụ trên. Ta cùng tìm hiểu phương trình hóa học của loại phản ứng này:
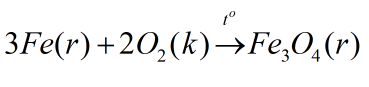
Đặc biệt lưu ý: 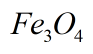 là hợp chất biểu diễn chung cho Sắt II và Sắt III và được gọi bởi cái tên: Oxit sắt từ
là hợp chất biểu diễn chung cho Sắt II và Sắt III và được gọi bởi cái tên: Oxit sắt từ
Oxi tác dụng với hợp chất
Ngoài đời thực ta thường thấy rất nhiều phản ứng của oxi với hợp chất. Tuy nhiên phổ biến nhất vẫn là phản ứng cháy của khí metan (có trong bùn ao, khí bioga) với oxi, tỏa nhiều nhiệt:
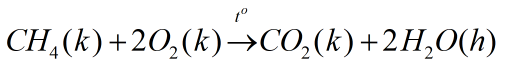
Trước khi bước vào một số bài tập thì chúng ta cùng tóm gọn lại tính chất của oxi mà các bạn học sinh lớp 8 cần phải nhớ:

Bài tập chương oxi có lời giải chi tiết
Câu 1: Nung nóng kali clorat KClO3 thu được 3,36 lít khí oxi trong điều kiện tiêu chuẩn, thực hiện các yêu cầu sau:
- Viết phương trình phản ứng cháy dựa vào tính chất hóa học của oxi đã học
- Tính khối lượng KClO3 cần dùng.
Lời giải:
a) Viết phương trình phản ứng: 2.KClO3 —to-> 2KCl +3O2
b) Tính khối lượng:
2.KClO3 —to-> 2KCl +3O2
2 mol 3 mol
x mol 0,15 mol
Khối lượng của KClO3 cần dùng là: m = n.M =0,1×122.5 = 12.25 (g)
Câu 2: Một oxit có chứa 50% Oxi phần còn lại là một nguyên tố khác. Tìm nguyên tố đó biết khối lượng mol của oxit là 64.
Lời giải:
% nguyên tố còn lại là: 100% – 50 % = 50 %
Khối lượng mol của nguyên tố cần tìm là: 64/2 = 32 => Nguyên tố cần tìm là S.
Câu 3:
Đốt cháy 12,4 (g) (P) trong bình chứa khí oxi.
a. Viết phương trình hóa học xảy ra cho phản ứng đốt cháy trên.
b.Tính thể tích khí oxi ở điều kiện tiêu chuẩn cần dùng để đốt cháy hết lượng (P) trên.
Lời giải:
a) Phương trình phản ứng: 4P + 5.O2 –to-> 2P2O5
b) Số mol Photpho (P) tham gia phản ứng: n(P) = 12.4/31 = 0.4 (mol)
4P + 5.O2 –to-> 2P2O5
4 mol 5 mol 2 mol
0.4 mol —> 0.5 mol
Thể tích khí Oxi cần dùng để đốt hết lượng Photpho mà đầu bài cho là:
V(O2) = 0.5×22.4 = 11,2 (lít)
Vậy là chúng ta vừa tìm hiểu xong khá nhiều vấn đề liên quan đế nguyên tố oxi như: Tính chất hóa học của oxi, tính chất vật lí và cả một số bài tập thường gặp trong chương trình hóa học lớp 8. Mong rằng với lượng kiến thức trên có thể giúp các em hiểu hơn về nguyên tố này trong cuộc sống cũng như những dạng bài tập hóa học khó.
Bản quyền bài viết thuộc trường Mầm Non Ánh Dương. Mọi hành vi sao chép đều là gian lận.
Nguồn chia sẻ: Trường Mầm Non Ánh Dương (mamnonanhduongvt.edu.vn)
Source: Mamnonanhduongvt.edu.vn
Category: Giáo dục