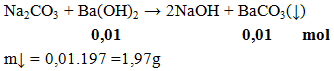Phản ứng Na2CO3 + Ba(OH)2 = 2NaOH + BaCO3 | Cân Bằng Phương Trình Hóa Học
Na2CO3 | natri cacbonat | dd + Ba(OH)2 | Bari hidroxit | dd = NaOH | natri hidroxit | dd + BaCO3 | Bari cacbonat | kt, Điều kiện
Na2CO3 + Ba(OH)2 → 2NaOH + BaCO3
Na2CO3 + Ba(OH)2 → 2NaOH + BaCO3 là Phản ứng trao đổi, Na2CO3 (natri cacbonat) phản ứng với Ba(OH)2 (Bari hidroxit) để tạo ra NaOH (natri hidroxit), BaCO3 (Bari cacbonat) dười điều kiện phản ứng là Không có
Điều kiện phản ứng để Na2CO3 (natri cacbonat) tác dụng Ba(OH)2 (Bari hidroxit) là gì ?
Không có
This post: Na2CO3 + Ba(OH)2 → 2NaOH + BaCO3
Làm cách nào để Na2CO3 (natri cacbonat) tác dụng Ba(OH)2 (Bari hidroxit)?
Nhỏ vài giọt dung dịch muối Na2CO3 vào ống nghiệm đựng 1ml dung dịch Ba(OH)2
Nếu đang làm bài tập các bạn có thể viết đơn giản là Na2CO3 (natri cacbonat) tác dụng Ba(OH)2 (Bari hidroxit) và tạo ra chất NaOH (natri hidroxit), BaCO3 (Bari cacbonat)
Hiện tượng nhận biết nếu phản ứng xảy ra Na2CO3 + Ba(OH)2 → 2NaOH + BaCO3 là gì ?
Xuất hiện kết tủa trắng BaCO3 trong dung dịch.
Thông tin nào cần phải lưu ý thêm về phương trình phản ứng Na2CO3 + Ba(OH)2 → 2NaOH + BaCO3
dung dịch muối có thể tác dụng với dung dịch bazơ tạo thành muối mới và bazơ mới.
Phương Trình Điều Chế Từ Na2CO3 Ra NaOH
Trong thực tế, sẽ có thể nhiều hơn 1 phương pháp điều chế từ Na2CO3 (natri cacbonat) ra NaOH (natri hidroxit)
Phương Trình Điều Chế Từ Na2CO3 Ra BaCO3
Trong thực tế, sẽ có thể nhiều hơn 1 phương pháp điều chế từ Na2CO3 (natri cacbonat) ra BaCO3 (Bari cacbonat)
Phương Trình Điều Chế Từ Ba(OH)2 Ra NaOH
Trong thực tế, sẽ có thể nhiều hơn 1 phương pháp điều chế từ Ba(OH)2 (Bari hidroxit) ra NaOH (natri hidroxit)
Phương Trình Điều Chế Từ Ba(OH)2 Ra BaCO3
Trong thực tế, sẽ có thể nhiều hơn 1 phương pháp điều chế từ Ba(OH)2 (Bari hidroxit) ra BaCO3 (Bari cacbonat)
Giải thích chi tiết về các phân loại của phương trình Na2CO3 + Ba(OH)2 → 2NaOH + BaCO3
Phản ứng trao đổi là gì ?
Phản ứng hoá học trong đó các chất trao đổi cho nhau thành phần cấu tạo của nó. Từ sự trao đổi này, chúng hình thành nên những chất mới. Trong phản ứng trao đổi, số oxi hóa của các nguyên tố không thay đổi. Các phản ứng trao đổi không phải là phản ứng oxi hóa – khử.
Bài tập vận dụng
Câu 1: Nhỏ từ từ một vài giọt Na2CO3 vào ống nghiệm có chứa 1ml Ba(OH)2 thu được kết tủa có màu
A. trắng. B. đen. C. vàng. D. nâu đỏ.
Hướng dẫn giải
Na2CO3 + Ba(OH)2 → 2NaOH + BaCO3(↓)
BaCO3(↓) trắng
Đáp án A.
Câu 2:
Chất nào sau đây không thể phản ứng với Na2CO3?
A. Ba(OH)2. B. BaCl2. C. Ba(NO3)2. D, BaCO3.
Hướng dẫn giải
BaCO3 không phản ứng với Na2CO3.
Đáp án D.
Câu 3:
Khối lượng kết tủa thu được khi cho Na2CO3 phản ứng vừa đủ với 100ml Ba(OH)2 0,1M là
A. 2,33g. B. 2,17g. C.1,97g. D. 2,00g
Hướng dẫn giải
Đáp án C.
Source: Mamnonanhduongvt.edu.vn
Category: Phương Trình Hoá Học Lớp 9