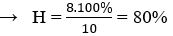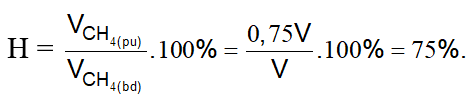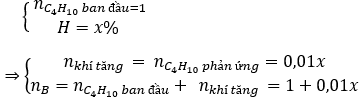C4H10 = C2H4 + C2H6 | Cân Bằng Phương Trình Hóa Học
C4H10 | Butan | khí = C2H4 | etilen (eten) | khí + C2H6 | etan | khí, Điều kiện Nhiệt độ nhiệt độ, Chất xúc tác xúc tác
Mục Lục
-
- Cách viết phương trình đã cân bằng
- Thông tin chi tiết về phương trình C4H10 → C2H4 + C2H6
- Điều kiện phản ứng để C4H10 (Butan) là gì ?
- Làm cách nào để C4H10 (Butan)?
- Hiện tượng nhận biết nếu phản ứng xảy ra C4H10 → C2H4 + C2H6 là gì ?
- Thông tin nào cần phải lưu ý thêm về phương trình phản ứng C4H10 → C2H4 + C2H6 ?
- Giải thích chi tiết về các phân loại của phương trình C4H10 → C2H4 + C2H6
- Phản ứng phân huỷ là gì ?
- Phản ứng Cracking là gì ?
- Phán ứng tách là gì ?
- Chuỗi phương trình hóa học có sử dụng C4H10 → C2H4 + C2H6
Cách viết phương trình đã cân bằng
 |
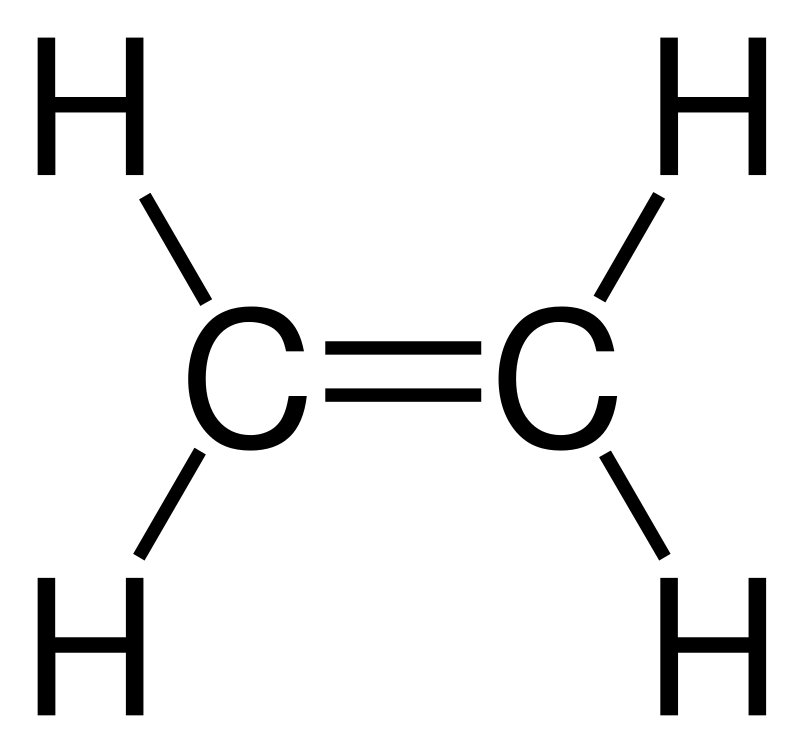 |
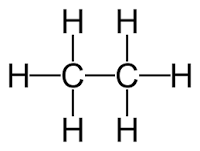 |
||
| C4H10 | → | C2H4 | + | C2H6 |
| Butan | etilen (eten) | etan | ||
| Ethene | ||||
| (khí) | (khí) | (khí) | ||
| (Không màu) | (Không màu) | (Không màu) | ||
| 58 | 28 | 30 |
Xin hãy kéo xuống dưới để xem và thực hành các câu hỏi trắc nghiệm liên quan
This post: C4H10 → C2H4 + C2H6
☟☟☟
Thông tin chi tiết về phương trình C4H10 → C2H4 + C2H6
C4H10 → C2H4 + C2H6 là Phản ứng phân huỷ, C4H10 (Butan) để tạo ra C2H4 (etilen (eten)), C2H6 (etan) dười điều kiện phản ứng là Nhiệt độ: nhiệt độ Xúc tác: xúc tác
Điều kiện phản ứng để C4H10 (Butan) là gì ?
Nhiệt độ: nhiệt độ Xúc tác: xúc tác
Làm cách nào để C4H10 (Butan)?
Chúng mình không thông tin về làm thế nào để C4H10 (Butan) và tạo ra chất C2H4 (etilen (eten)) phản ứng với C2H6 (etan).
Bạn có thể kéo xuống dưới và click vào nút báo lỗi để đóng góp thông tin cho chúng mình nhé.
Nếu đang làm bài tập các bạn có thể viết đơn giản là C4H10 (Butan) và tạo ra chất C2H4 (etilen (eten)), C2H6 (etan)
Hiện tượng nhận biết nếu phản ứng xảy ra C4H10 → C2H4 + C2H6 là gì ?
Phương trình không có hiện tượng nhận biết đặc biệt.
Trong trường hợp này, bạn chỉ thường phải quan sát chất sản phẩm C2H4 (etilen (eten)) (trạng thái: khí) (màu sắc: Không màu), C2H6 (etan) (trạng thái: khí) (màu sắc: Không màu), được sinh ra
Hoặc bạn phải quan sát chất tham gia C4H10 (Butan) (trạng thái: khí) (màu sắc: Không màu), biến mất.
Thông tin nào cần phải lưu ý thêm về phương trình phản ứng C4H10 → C2H4 + C2H6
Ở nhiệt độ cao và có mặt chất xúc tác thích hợp, ngoài việc bị tách hiđro, các ankan còn có thể bị phân cắt mạch cacbon tạo thành các phân tử nhỏ hơn.
Phương Trình Điều Chế Từ C4H10 Ra C2H4
Trong thực tế, sẽ có thể nhiều hơn 1 phương pháp điều chế từ C4H10 (Butan) ra C2H4 (etilen (eten))
Xem tất cả phương trình điều chế từ C4H10 (Butan) ra C2H4 (etilen (eten))
Phương Trình Điều Chế Từ C4H10 Ra C2H6
Trong thực tế, sẽ có thể nhiều hơn 1 phương pháp điều chế từ C4H10 (Butan) ra C2H6 (etan)
Xem tất cả phương trình điều chế từ C4H10 (Butan) ra C2H6 (etan)
Giải thích chi tiết về các phân loại của phương trình C4H10 → C2H4 + C2H6
Phản ứng phân huỷ là gì ?
Trong phản ứng phân hủy, số oxi hóa cuả các nguyên tố có thể thay đổi hoặc không thay đổi. Như vậy, phản ứng phân hủy có thể là phản ứng oxi hóa – khử hoặc không phải là phản ứng oxi hóa – khử. Phản ứng hoá học là loại phản ứng xuất hiện nhiều trong chương trình Hoá trung học cơ sở, phổ thông cho tới Ôn Thi Đại Học.
Xem tất cả phương trình Phản ứng phân huỷ
Phản ứng Cracking là gì ?
Người ta dùng phản ứng cracking đối với ankan có số cacbon trong phân tử từ 3 trở lên. Sản phẩm của phản ứng này là một ankan và một anken có số cacbon thấp hơn số cacbon của tác chất. Phương trình tổng quát như sau: CnH2n+2 —-cracking—> CmH2m + CkH2k+2 (với m+k=n, 2m+2k=2n, m<n, k<n,=”” n=””>=3)</n,>
Xem tất cả phương trình Phản ứng Cracking
Phán ứng tách là gì ?
Phản ứng tác là phản ứng trong đó hai hay nhiều nguyên tử bị tách ra khỏi phân tử hợp chất hữu cơ
Xem tất cả phương trình Phán ứng tách
Ví dụ minh họa
Ví dụ 1: Tiến hành cracking 10 lít khí butan, sau phản ứng thu được 18 lít hỗn hợp khí gồm etan, metan, eten, propylen, butan (các khí đo cùng điều kiện). Hiệu suất quá trình phản ứng cracking?
A. 60%
B. 70%
C. 80%
D. 90%
Hướng dẫn:
Cracking butan:
C4H10 → C2H6 + C2H4
C4H10 → CH4 + C3H6
Do các khí đo ở cùng điều kiện nên từ phản ứng, ta có:
V(sản phẩm) = 2.VC4H10(phản ứng) = 2x (lít)
⇒ VC4H10 (phản ứng) = V(khí tăng) = V(hỗn hợp sau phản ứng) – V(ban đầu)
Do đó: Vtăng = x (lít); V(hỗn hợp sau phản ứng) = 10 + x = 18 → x = 8 (lít)
Đáp án C.
Ví dụ 2: Thực hiện cracking V lít khí butan , thu được 1,75 lít hỗn hợp khí gồm 5 hidrocacbon. Hiệu suất phản ứng cracking butan? (các khí đo ở cùng điều kiện nhiệt độ và áp suất).
A. 80%
B. 25%
C. 75%
D. 50%
Hướng dẫn:
VC4H10 (phản ứng) = V(khí tăng) = 1,75V – V =0,75V (lít)
Đáp án C.
Ví dụ 3: Cracking butan (A) thu được hỗn hợp B gồm 5 hidrocacbon có khối lượng mol trung bình là 32,65 gam/mol. Hiệu suất phản ứng cracking?
A .77,64%
B. 38,82%
C. 17,76%
D. 16,325%
Hướng dẫn:
Theo định luật bảo toàn khối lượng: mA = mB
58 = 32,65.(1 + 0,01x)
X = 77,64 ⇒ H = 77,64%
Đáp án A.
Source: Mamnonanhduongvt.edu.vn
Category: Phương Trình Hoá Học Lớp 11