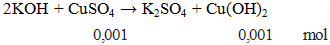Dưới đây Trường mầm non ánh dương cung cấp tài liệu về 2KOH + CuSO4 → Cu(OH)2 + K2SO4 | Cân Bằng Phương Trình Hóa Học KOH | kali hidroxit | lỏng + CuSO4 | Đồng(II) sunfat | lỏng = Cu(OH)2 | Đồng (II) hidroxit | rắn + K2SO4 | Kali sunfat | lỏng, Điều kiện Điều kiện khác nhiệt độ thường
Phương Trình Hoá Học Lớp 9 Phương Trình Hoá Học Lớp 10 Phương Trình Hoá Học Lớp 12 Phản ứng trao đổi Phương trình hóa học vô cơ Chuỗi Phương Trình Lớp 12
This post: 2KOH + CuSO4 → Cu(OH)2 + K2SO4 | Cân Bằng Phương Trình Hóa Học
Cách viết phương trình đã cân bằng
| 2KOH | + | CuSO4 | → | Cu(OH)2 | + | K2SO4 |
| kali hidroxit | Đồng(II) sunfat | Đồng (II) hidroxit | Kali sunfat | |||
| Copper(II) sulfate | Copper(II) hydroxide | Potassium sulfate | ||||
| (lỏng) | (lỏng) | (rắn) | (lỏng) | |||
| (không màu) | (xanh lam) | (xanh) | (không màu) | |||
| Bazơ | Muối | Muối | Muối | |||
| 56 | 160 | 98 | 174 |
Phương trình phản ứng: 2KOH + CuSO4 → Cu(OH)2 + K2SO4
2KOH + CuSO4 → Cu(OH)2 + K2SO4 là Phản ứng trao đổi, KOH (kali hidroxit) phản ứng với CuSO4 (Đồng(II) sunfat) để tạo ra Cu(OH)2 (Đồng (II) hidroxit), K2SO4 (Kali sunfat) dười điều kiện phản ứng là Điều kiện khác: nhiệt độ thường
- Điều kiện phản ứng để KOH (kali hidroxit) tác dụng CuSO4 (Đồng(II) sunfat) là gì ?
Điều kiện khác: nhiệt độ thường
- Làm cách nào để KOH (kali hidroxit) tác dụng CuSO4 (Đồng(II) sunfat)?
Nhỏ từ từ dung dịch KOH vào ống nghiệm đựng dung dịch muối đồng (II) sunfat.
Nếu đang làm bài tập các bạn có thể viết đơn giản là KOH (kali hidroxit) tác dụng CuSO4 (Đồng(II) sunfat) và tạo ra chất Cu(OH)2 (Đồng (II) hidroxit), K2SO4 (Kali sunfat)
- Hiện tượng nhận biết nếu phản ứng xảy ra 2KOH + CuSO4 → Cu(OH)2 + K2SO4 là gì ?
Xuất hiện kết tủa màu xanh
Ứng dụng thực tế 2KOH + CuSO4 → Cu(OH)2 + K2SO4
- Phương Trình Điều Chế Từ KOH Ra Cu(OH)2
Trong thực tế, sẽ có thể nhiều hơn 1 phương pháp điều chế từ KOH (kali hidroxit) ra Cu(OH)2 (Đồng (II) hidroxit)
- Phương Trình Điều Chế Từ KOH Ra K2SO4
Trong thực tế, sẽ có thể nhiều hơn 1 phương pháp điều chế từ KOH (kali hidroxit) ra K2SO4 (Kali sunfat)
- Phương Trình Điều Chế Từ CuSO4 Ra Cu(OH)2
Trong thực tế, sẽ có thể nhiều hơn 1 phương pháp điều chế từ CuSO4 (Đồng(II) sunfat) ra Cu(OH)2 (Đồng (II) hidroxit)
- Phương Trình Điều Chế Từ CuSO4 Ra K2SO4
Trong thực tế, sẽ có thể nhiều hơn 1 phương pháp điều chế từ CuSO4 (Đồng(II) sunfat) ra K2SO4 (Kali sunfat)
Câu hỏi trắc nghiệm và bài tập liên quan 2KOH + CuSO4 → Cu(OH)2 + K2SO4
Ví dụ 1:
Nhỏ từ từ dung dịch KOH vào ống nghiệm chứa CuSO4. Hiện tượng thu được sau phản ứng là
A. xuất hiện kết tủa trắng.
B. xuất hiện kết tủa nâu đỏ.
C. xuất hiện kết tủa sau đó kết tủa tan.
D. xuất hiện kết tủa xanh.
Hướng dẫn giải
2KOH + CuSO4 → K2SO4+ Cu(OH)2
Cu(OH)2: kết tủa xanh.
Đáp án D.
Ví dụ 2:
Phản ứng nào sau đây là phản ứng trao đổi?
A. KOH + CO2 → KHCO3
B. 2KOH + CO2 → K2CO3+ H2O
C. 2K + 2HCl → 2KCl + H2
D. 2KOH + CuSO4 → K2SO4 + Cu(OH)2
Hướng dẫn giải
2KOH + CuSO4 → K2SO4 + Cu(OH)2 là phản ứng trao đổi.
Đáp án D.
Ví dụ 3:
Cho 100ml CuSO4 0,01M phản ứng vừa đủ với dung dịch KOH thu được kết tủa X. Khối lượng kết tủa X là
A. 0,098g. B. 0,98g. C. 0,754g. D. 1,10g.
Hướng dẫn giải
mmuối = 0,001.98 = 0,098gam.
Đáp án A.
Mời các bạn tham khảo một số tài liệu quan
→ Xem thêm: Hướng dẫn cách cân bằng phương trình C2H4 + H2O → C2H5OH
………………………
Mầm Non Ánh Dương đã gửi tới bạn phương trình hóa học 2KOH + CuSO4 → Cu(OH)2 + K2SO4, khi cho dung dịch KOH (kali hidroxit) phản ứng với CuSO4 (Đồng(II) sunfat) để tạo ra Cu(OH)2 (Đồng (II) hidroxit), K2SO4 (Kali sunfat). Hy vọng với tài liệu này sẽ cung cấp các thông tin cần thiết cho các bạn.
Ngoài ra, Mầm Non Ánh Dương đã thành lập group chia sẻ tài liệu học tập THPT miễn phí trên Facebook: Tài liệu học tập lớp 11. Mời các bạn học sinh tham gia nhóm, để có thể nhận được những tài liệu mới nhất.
Chúc các bạn học tập tốt.
Source: Mamnonanhduongvt.edu.vn
Category: Phương Trình Hoá Học Lớp 9