Lý Thuyết Phản Ứng Oxi Hóa Khử Lớp 10 Và Giải Bài Tập SGK Trang 83
I. Phản ứng oxi hóa – khử lớp 10
Phản ứng oxi hóa khử là phản ứng hóa học, trong đó có sự chuyển electron giữa các chất trong phản ứng hay phản ứng oxi hóa khử là phản ứng hóa học trong đó có sự thay đổi số oxi hóa của một số nguyên tố.
This post: Phản ứng oxi hóa khử
– Chất khử (chất bị oxh) là chất nhường electron
– Quá trình oxh (sự oxh) là quá trình nhường electron.
– Quá trình khử (sự khử) là quá trình thu electron.
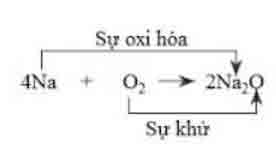
Ví dụ:
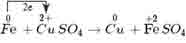
Quá trình thay đổi số oxi hóa:
Fe0→ Fe2++ 2e
– Nguyên tử sắt là chất khử. Sự làm tăng số oxi hóa của sắt được gọi là sự oxi hóa nguyên tử sắt.
– Nguyên tử sắt nhường electron, là chất khử. Sự nhường electron của nguyên tử sắt được gọi là sự oxi hóa nguyên tử sắt.
Cu2++ 2e → Cu
– Số oxi hóa của đồng giảm từ +2 xuống 0. Ion đồng là chất oxi hóa. Sự làm giảm số oxi hóa của ion đồng được gọi là sự khử ion đồng.
– Ion đồng nhận electron, là chất oxi hóa. Sự nhận electron của ion đồng được gọi là sự khử ion đồng.
⇒ Phản ứng của sắt với dung dịch đồng sunfat cũng là phản ứng oxi hóa – khử vì tồn tại đồng thời sự oxi hóa và sự khử.
II. Lập phương trình hóa học của phản ứng oxi hóa khử lớp 10
Bước 1:Xác định số oxi hóa của các nguyên tố để tìm chất oxi hoá và chất khử.
Bước 2:Viết quá trình oxi hóa và quá trình khử, cân bằng mỗi quá trình.
Bước 3:Tìm hệ số thích hợp cho chất oxh và chất khử sao cho tổng số electron cho bằng tổng số electron nhận.
Bước 4:Đặt hệ số của các chất oxh và khử vào sơ đồ phản ứng, từ đó tính ra hệ số các chất khác. Kiểm tra cân bằng số nguyên tử của các nguyên tố và cân bằng điện tích hai vế để hoàn thành PTHH.
III. Ý nghĩa của phản ứng oxi hóa khử lớp 10
– Phản ứng oxi hóa – khử là một trong những quá trình quan trọng nhất của thiên nhiên:
Sự hô hấp, quá trình thực vật hấp thụ khí cacbonic giải phóng oxi, sự trao đổi chất và hàng loạt quá trình sinh học khác đều có cơ sở là các phản ứng oxi hóa – khử.
– Ngoài ra: Sự đốt cháy nhiên liệu trong các động cơ, các quá trình điện phân, các phản ứng xảy ra trong pin và trong ăcquy đều bao gồm sự oxi hóa và sự khử.
Hàng loạt quá trình sản xuất như luyện kim, chế tạo hóa chất, chất dẻo, dược phẩm, phân bón hóa học, … đều không thực hiện được nếu thiếu các phản ứng oxi hóa – khử.
IV. Hướng dẫn giải bài tập phản ứng oxi hóa khử lớp 10 trang 83.

Còn các phản ứng khác không phải là phản ứng oxi hóa khử
Bài 2:Cho các phản ứng sau:
A. 4NH3+ 5O2→ 4NO + 6H2O.
B. 2NH3+ 3Cl2→ N2+ 6HCl.
C. 2NH3+ 3CuO → 3Cu + N2+ 3H2O.
D. 2NH3+ H2O2+ MnSO4→ MnO2+ (NH4)2SO4.
Ở phản ứng nào NH3không đóng vai trò chất khử?
Lời giải:
Phản ứng NH3không đóng vai trò chất khử.D. 2NH3+ H2O2+ MnSO4→ MnO2+ (NH4)2SO4.
Do N không thay đổi số oxi hóa trước và sau phản ứng.
Bài 3:Trong số các phản ứng sau:
A. HNO3+ NaOH → NaNO3+ H2O.
B. N2O5+ H2O → 2HNO3.
C. 2HNO3+ 3H2S → 3S + 2NO + 4H2O.
D. 2Fe(OH)3→ Fe2O3+ 3H2O.
Phản ứng nào là phản ứng oxi hóa – khử.
Lời giải:
Trong các phản ứng trên chỉ có phản ứng C là phản ứng oxi hóa – khử vì có sự thay đổi số oxi hóa của các nguyên tố.
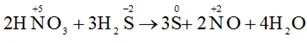
Bài 4:Trong phản ứng 3NO2+ H2O → 2HNO3+ NO. NO2đóng vai trò gì?
A. Chỉ là chất oxi hóa.
B. Chỉ là chất khử.
C. Là chất oxi hóa, nhưng đồng thời cũng là chất khử.
D. Không là chất oxi hóa, không là chất khử.
Chọn đáp án đúng.
Lời giải:
NO2đóng vai trò vừa là chất oxi hóa vừa là chất khử: C đúng
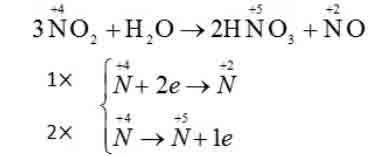
Bài 5:Phân biệt chất oxi hóa và sự oxi hóa, chất khử và sự khử. Lấy thí dụ để minh họa.
Lời giải:
Chất oxi hóa là chất nhận electron.
Sự oxi hóa một chất là làm cho chất đó nhường electron.
Chất khử là chất nhường electron.
Sự khử một chất là sự làm cho chất đó thu electron.
Ví dụ:
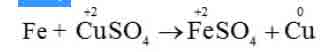
– Nguyên tử Fe nhường electron, là chất khử. Sự nhường electron của Fe được gọi là sự oxi hóa nguyên tử sắt.
– Ion đồng nhận electron, là chất oxi hóa. Sự nhận electron của ion đồng được gọi là sự khử ion đồng.
Bài 6:Thế nào là phản ứng oxi hóa – khử? Lấy ba thí dụ.
Lời giải:
Phản ứng oxi hóa – khử là phản ứng hóa học trong đó có sự chuyển electron giữa các chất phản ứng.
Thí dụ:
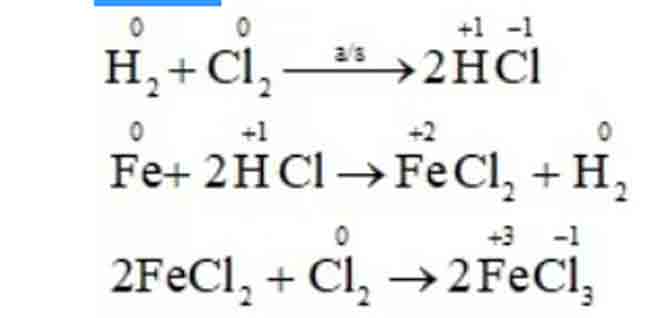
Bài 7:Lập phương trình phản ứng oxi hóa – khử sau đây theo phương pháp thăng bằng electron:a) Cho MnO2tác dụng với dung dịch axit HCl đặc, thu được MnCl2, Cl2và H2
b) Cho Cu tác dụng với dung dịch axit HNO3đặc, nóng thu được Cu(NO3)2, NO2, H2
c) Cho Mg tác dụng với dung dịch axit H2SO4đặc, nóng thu được MgSO4, S và H2
Lời giải:
Các phương trình hóa học là.
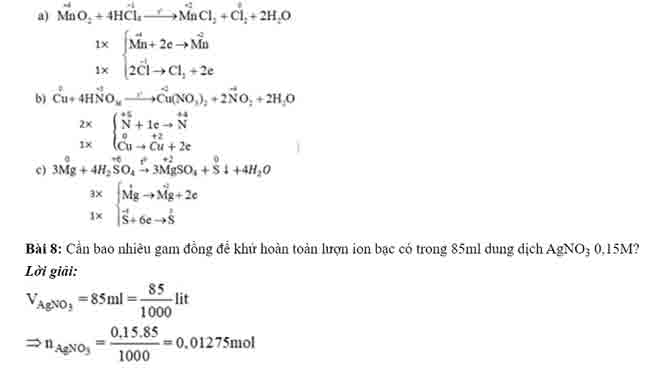
Phương trình hóa học của phản ứng:
Cu + 2AgNO3→ Cu(NO3)2+ 2Ag
Theo pt:
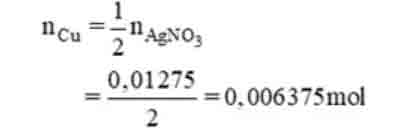
mCutham gia phản ứng: 0,006375 × 64 = 0,408 g.
Bài Tập Cân Bằng Phản Ứng Oxi hóa Khử
Phản ứng oxi hoá khử, cách lập phương trình hoá học và bài tập – hoá 10 bài 17
Bài 17. Phản ứng oxi hóa – khử
Phản ứng oxi hóa -khử
I. KHÁI NIỆM
- Phản ứng oxi hoá – khử
- Khái niệm: Phản ứng oxi hóa – khử là phản ứng hoá học trong đó có sự chuyển electron giữa các chất phản ứng.
- Dấu hiệu nhận biết: Phản ứng có sự thay đổi số oxi hóa của một số nguyên tố.
- Chất khử (chất bị oxi hoá)
- Khái niệm: Chất khử là chất có khả năng nhường e (cho e).
- Dấu hiệu nhận biêt:
- Sau phản ứng, số oxi hoá của chất khử tăng.
- Chất khử có chứa nguyên tố chưa đạt đến mức oxi hoá cao nhất.
Chú ý: Nguyên tố ở nhóm XA có số oxi hoá cao nhất là +X.
- Chất oxi hoá (chất bị khử)
- Khái niệm: Chất oxi hoá là chất có khả năng nhận e (thu e).
- Dấu hiệu:
- Sau phản ứng, số oxi hoá của chất oxi hoá giảm.
- Chất oxi hoá có chứa nguyên tố có mức oxi hoá chưa phải thấp nhất.
Chú ý: Kim loại có số oxi hoá thấp nhất là 0, phi kim thuộc nhóm xA thì số oxi hoá thấp nhất là (x – 8).
- Sự khử và sự oxi hoá
- Sự khử (quá trình khử) của một chất là làm cho chất đó nhận electron hay làm giảm số oxi hoá của chất đó.
- Sự oxi hoá (quá trình oxi hoá) của một chất là làm cho chất đó nhường electron hay làm tăng số oxi hoá của chất đó.
II. ĐIỀU KIỆN CỦA PHẢN ỨNG OXI HOÁ – KHỬ
Phải có sự tham gia đồng thời của chất khử và chất oxi hóa. Chất khử và chất oxi hóa phải đủ mạnh.
III. PHÂN LOẠI PHẢN ỨNG OXI HOÁ – KHỬ
Phản ứng oxi hoá – khử được chia thành nhiều loại khác nhau:
– Phản ứng oxi hóa – khử thông thường: chất khử và chất oxi hóa ở 2 phân tử chất khác nhau.
C + 4HNO3đặc →CO2+ 4NO2+ 2H2O
Cu + 2H2SO4đặc→CuSO4+ SO2+ 2H2O
– Phản ứng oxi hóa – khử nội phân tử:chất khử và chất oxi hóa thuộc cùng 1 phân tử nhưng ở 2 nguyên tử khác nhau (thường gặp là phản ứng nhiệt phân).
AgNO3→Ag + NO2+ O2
Cu(NO3)2→CuO + NO2+ O2
– Phản ứng tự oxi hóa – khử, chất khử đồng thời cũng là chất oxi hóa (chất khử và chất oxi hoá thuộc về cùng một nguyên tố trong một phân tử chất).
Cl2+ 2NaOH→NaCl + NaClO + H2O
2NO2+ 2NaOH→NaNO2+ NaNO3+ H2O
4KClO3→3KClO4+ KCl
Bản quyền bài viết thuộc trường Mầm Non Ánh Dương. Mọi hành vi sao chép đều là gian lận.
Nguồn chia sẻ: Trường Mầm Non Ánh Dương (mamnonanhduongvt.edu.vn)
Source: Mamnonanhduongvt.edu.vn
Category: Tin Tức